Генетическое тестирование при хроническом панкреатите
В отделение неотложной помощи госпитализирована 26-летняя жительница штата Гулжарат (Индия) на девятом месяце первой беременности с рвотой и лихорадкой, жалобами на сильную боль в эпигастрии, иррадиирующую в поясницу.
В анамнезе не было указаний на желчнокаменную болезнь, приём лекарств и алкоголя.
Семейный анамнез не отягощён хроническим панкреатитом, муковисцидозом, гиперлипидемией и абдоминальным болевым синдромом.
В анализах: повышенный уровень амилазы при нормальном содержании кальция, нормальном липидном спектре и нормальной функции почек.
УЗИ брюшной полости не выявило желчных камней.
Из крови высеяна Klebsiella.
Срочно проведено кесарево сечение, ребёнок здоровый, мать провела 14 дней в отделение интенсивной терапии.
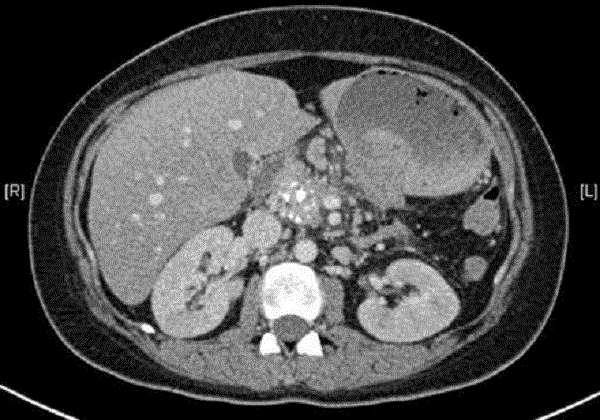
Компьютерная томография: очаговый интерстициальный панкреатит с обширной кальцификацией и большим воспалительным инфильтратом в хвосте поджелудочной железы вокруг расширенного панкреатического протока.
Повторно госпитализирована через два месяца с приступом острого панкреатита и рецидивом септицемией Klebsiella, но и после выписки испытывала боли в животе в течение всего следующего года.
Третья госпитализация по поводу приступа острого панкреатита в местное гепатологическое отделение.
При поступлении в норме клинический анализ крови, анализ мочи и содержание электролитов. СРБ 19, амилаза 130, антинейтрофильные цитоплазматические антитела к протеиназе 3 - 40 (норма <26), антитела к b-2 гликопротеину I класса IgG - 11 (норма <7).
Исследование крови на малярийные плазмодии, посев крови, исследования на ревматоидный фактор, антитела к кардиолипину класса IgM, антитела к внутреннему фактору миелопероксидазе, антитела к базальной мембране клубочков, антинуклеарный фактор Hep-2 и тесты на ВИЧ отрицательны.
Уровни компонентов системы комплемента С3 и С4 в норме.
При КТ брюшной полости выявлены очаги острого воспаления на фоне хронического панкреатита с обширной кальцификацией тела и головки, большой воспалительный инфильтрат в области расширенного панкреатического протока хвоста.
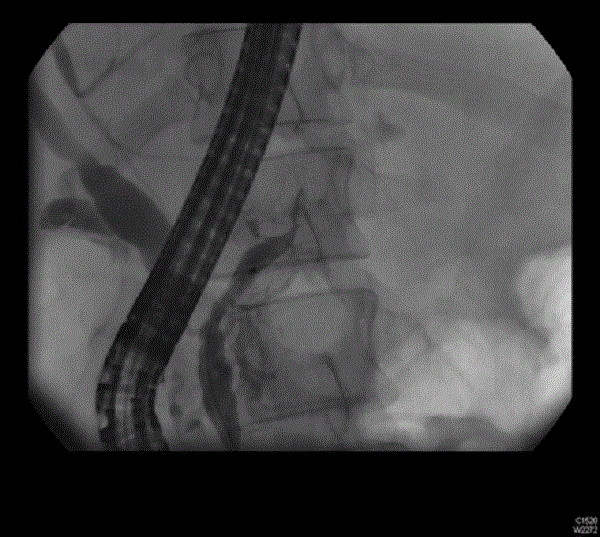
Эндоскопическая ретроградная холангиопанкреатография не удалась из-за повреждения протока проксимальной части тела поджелудочной железы.
Предположено наличие рака хвоста поджелудочной железы на фоне хронического панкреатита.
Пациентка испытывала постоянную сильную боль в эпигастральной области, резистентную к медикаментозной терапии.
Выполнена лапароскопическая дистальная резекция поджелудочной железы, селезёнка сохранена.
Обнаружено тяжёлое воспаление хвоста поджелудочной железы с обширным инфильтратом, в который вовлекается брыжейка толстой кишки, желудок и сосуды селезенки.
Гистология: полное замещение паренхимы поджелудочной железы фиброзной тканью, без злокачественных изменений.
Послеоперационный период без осложнений, выписана на 5 день.
В течение шести недель амбулаторного наблюдения не было жалоб, анальгетиков не принимала.
При генетическом тестировании выявлена мутация N34S в гене SPINK-1 (панкреатический секреторный ингибитор трипсина, тип Kazal-1); без мутации R122H и N34S в гене PRSS1 (катионический трипсиноген).
Алкоголь является самым частым этиологическим фактором развития хронического панкреатита, но треть случаев считаются идиопатическими.
В этой группе нередко выявляется генетическая предрасположенность: мутация N34S в гене SPINK-1 (панкреатический секреторный ингибитор трипсина, тип Kazal-1), ген CTFR (регулятор трансмембранной проводимости при муковисцидозе) и мутации R122H и N291 в гене PRSS1 (катионический трипсиноген).
SPINK-1 снижает вероятность развития панкреатита, предотвращая преждевременный аутолиз трипсина и уменьшая его активность на 20%.
Мутация N34S обнаруживается у 13-37% пациенток с внутрипеченочным холестазом беременных по сравнению с 2,5-5,1% в популяции.
Крупнейшее исследование EUROPAC включило 527 больных наследственным панкреатитом: 82% из 399 генетически протестированных имели мутации в гене PRSS1, среди которых самой распространенной была R122H.
Риск развития рака поджелудочной железы составил
- 1,5% в 20 лет;
- 2,5% в 30 лет;
- 8,5% в 40 лет;
- 14,6% в 50 лет;
- 25,3% в 60 лет и
- 44% в 70 лет, но при наличии мутации в PRSS1 риск изменялся незначительно.
При хроническом панкреатите на КТ сложно дифференцировать злокачественное и воспалительное поражение, но 12% изолированных стриктур панкреатических протоков оказываются злокачественными.
Исследование EUROPAC показало, что при наследственном хроническом панкреатите кальцификация свидетельствует о повышении риска рака.
В приведённом случае не выполнена тотальная панкреатэктомия, так как у пациентки была выявлена мутация N34S в SPINK-1 без мутации в гене PRSS1.
Перевод Анны Абрамовой
